Anvisa libera Mounjaro para crianças com diabetes tipo 2
Medicamento à base de tirzepatida tornou-se o primeiro e único GLP-1 aprovado para pacientes pediátricos
 por César Ferro em e atualizado em
por César Ferro em e atualizado em 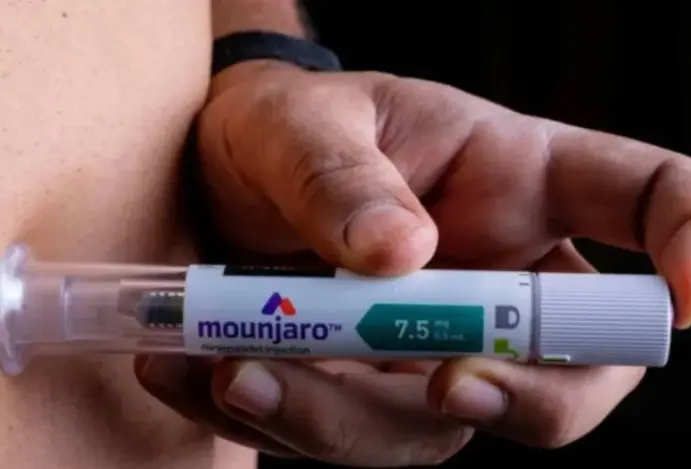
Nesta quarta-feira, dia 22, a Anvisa aprovou o Mounjaro para o tratamento do diabetes tipo 2 em crianças e adolescentes de 10 a 17 anos. O medicamento da Eli Lilly à base de tirzepatida já é aprovado no Brasil para adultos no tratamento da doença, no controle crônico do peso em pacientes com obesidade ou sobrepeso com comorbidades e na apneia obstrutiva do sono moderada a grave em adultos com obesidade. Com a decisão, ele passa a ser o primeiro e único agonista duplo dos receptores GIP/GLP-1 aprovado para uso em pacientes pediátricos.
A doença, historicamente associada à vida adulta, tornou-se uma epidemia silenciosa entre crianças e adolescentes brasileiros. O País figura entre os dez com maior número de casos na faixa etária pediátrica no mundo.
Dados da Sociedade Brasileira de Diabetes estimam que cerca de 213 mil adolescentes vivam com a condição no Brasil, além de outros 1,46 milhão em situação de pré-diabetes. Esse aumento está diretamente associado à epidemia de obesidade infantil: atualmente, um em cada três adolescentes brasileiros tem excesso de peso, e estima-se que cerca de um terço das novas crianças diagnosticadas apresente esse tipo da doença.
Mounjaro para pacientes pediátricos representa “avanço da ciência”
Para Luiz André Magno, diretor médico sênior da Lilly, a aprovação do Mounjaro para pacientes pediátricos representa um avanço científico com impacto social. “Crianças e adolescentes com diabetes tipo 2 enfrentam uma progressão mais rápida da doença do que adultos, e as opções disponíveis até então apresentavam limitações no controle glicêmico”, aponta.
A aprovação da Anvisa se baseia nos resultados do estudo clínico de fase 3 SURPASS-PEDS, publicado em setembro de 2025 no periódico The Lancet. O estudo atingiu o desfecho primário ao demonstrar redução superior da hemoglobina glicada com doses agrupadas de tirzepatida em comparação ao placebo, ao longo de 30 semanas. A redução média foi de 2,2 pontos percentuais, a partir de uma linha basal média de 8,05% usando a eficácia estimada.
Em um desfecho secundário, 86,1% dos participantes que receberam 10 mg do medicamento atingiram o nível alvo de ≤ 6,5%. Além disso, o tratamento demonstrou melhorias clínicas no IMC: a dose mais alta reduziu o índice em média 11,2% em 30 semanas. Esses resultados se mantiveram por até 52 semanas na extensão de longo prazo do estudo.
O perfil de segurança observado foi consistente com o já conhecido para a classe de incretinas, incluindo dados anteriores do programa SURPASS. As taxas de descontinuação por eventos adversos foram baixas, e não houve registro de hipoglicemia grave durante o estudo.
Agência propôs regras mais rígidas para manipulação
Pouco antes de confirmar a aprovação do Mounjaro para crianças, a Anvisa publicou uma minuta de proposta que estabelece regras mais rígidas para a manipulação de medicamentos à base de tirzepatida. O texto será analisado pela Diretoria Colegiada na próxima quarta-feira, dia 29, e foca no controle de insumos farmacêuticos ativos (IFAs) agonistas e coagonistas do receptor GLP-1/GIP.
A medida surge como resposta ao volume expressivo de importações identificado pela autarquia. Dados do órgão indicam que, entre novembro de 2025 e abril de 2026, a entrada do princípio ativo no país superou 100 quilos – quantidade suficiente para a produção de mais de 20 milhões de doses de 5 mg.