Terapia gênica é aprovada para anemia falciforme
 por Ana Claudia Nagao em
por Ana Claudia Nagao em 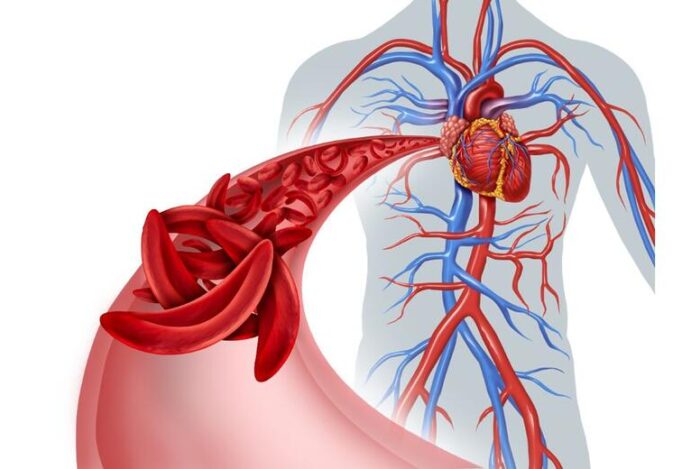
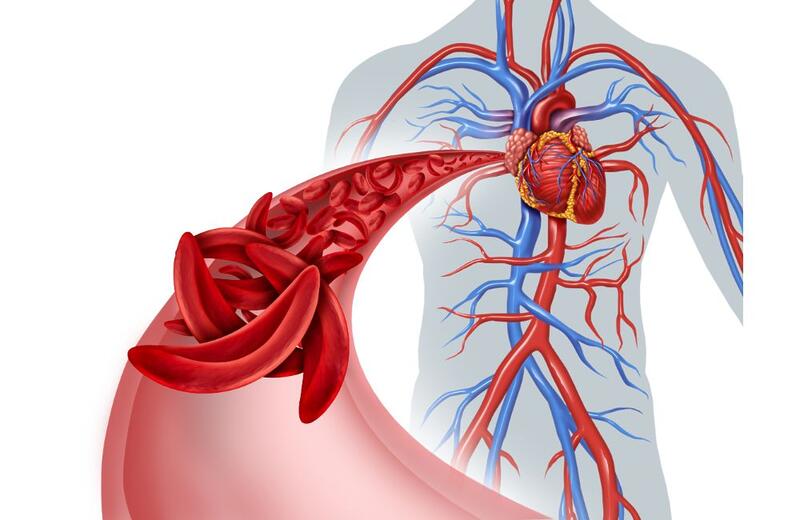
A primeira terapia gênica do mundo no tratamento da anemia falciforme e talassemia foi autorizada pela Agência Reguladora de Medicamentos e Produtos de Saúde do Reino Unido. A terapia, batizada de Casgevy, foi desenvolvida em parceria pelas empresas farmacêuticas Vertex e CRISPR Therapeutics. Ela utiliza a tecnologia CRISPR/Cas9, uma técnica de edição gênica que realiza cortes precisos no DNA do paciente. As informações são do Estado de Minas e da Global Data.
A aprovação ocorreu por meio de uma autorização condicional, que ocorre em casos específicos, com dados menos abrangentes de estudos clínicos, quando os benefícios imediatos superam os riscos. A expectativa é que essa autorização se torne definitiva assim que a farmacêutica responsável apresentar estudos mais amplos.
Quais pacientes com anemia falciforme podem fazer uso da terapia?
A autorização para o uso da Casgevy foi concedida a pacientes com mais de 12 anos que apresentem crises vaso-oclusivas recorrentes (entupimento dos vasos sanguíneos, causando dor intensa) e para os quais o transplante de medula óssea seja indicado, mas não haja um doador compatível disponível.
A agência reguladora também aprovou a mesma terapia para pacientes com talassemia beta, outra doença hereditária, que sejam dependentes de transfusão sanguínea e não tenham conseguido encontrar um doador compatível para o transplante de medula.
Segundo a farmacêutica Vertex, em dois ensaios clínicos globais, a terapia gênica alcançou os resultados primários esperados, livrando os pacientes de crises vaso-oclusivas graves e tornando-os livres de transfusões de sangue por 12 meses consecutivos. Espera-se que esses resultados perdurem pelo resto da vida. Em comunicado, a empresa informou que está trabalhando com as autoridades de saúde para garantir o acesso dos pacientes elegíveis o mais rápido possível. A mesma terapia está sob análise da FDA (agência norte-americana reguladora de fármacos e alimentos), e a decisão deve ser anunciada em dezembro.
“A aprovação do Casgevy para anemia falciforme e talassemia beta anuncia uma nova era em que o potencial de curar doenças genéticas se torna uma realidade tangível, oferecendo esperança a milhões de pessoas em todo o mundo que lutam contra condições hereditárias”, afirma Joselia Carlos, analista de Dispositivos Médicos da GlobalData.
Mercado de terapia gênica e celulat
O mercado global de terapia celular e gênica deve atingir US$ 80 bilhões em 2029, com uma alta taxa composta de crescimento anual de 51,6% entre 2023 e 2029, de acordo com previsões da GlobalData. A Vertex Pharmaceuticals provavelmente ganhará uma posição dominante no mercado global de terapia celular e gênica.
“O fator limitante para o uso generalizado desse medicamento é seu alto custo. Estimativas sugerem que pode custar aproximadamente US$ 2 milhões por paciente. Para reduzir os custos da Casgevy e garantir sua segurança e eficácia, pesquisas contínuas, supervisão ética e colaboração entre cientistas, formuladores de políticas e prestadores de serviços de saúde são imperativos”, finaliza Joselia.
Este conteúdo é meramente informativo e não substitui a consulta médica. Para esclarecimento de dúvidas adicionais sobre uma patologia, medicamento ou tratamento, converse com um profissional de saúde de sua confiança. Evite sempre a automedicação.